Gli antibiotici rivestono grande importanza nella terapia animale ma anche umana, dunque il loro effetto deve permanere e l’emergenza dell’antibiotico-resistenza va contenuta. Inoltre, sempre maggiori pressioni da parte dell’opinione pubblica spingono gli addetti al settore zootecnico a ridimensionare il management del farmaco. Alla luce della mancanza di nuove molecole che possano tamponare il problema delle resistenza batterica, l’approccio da valutare è certamente un utilizzo razionale degli antibiotici a disposizione e l’affiancamento di strumenti non-farmacologici di management, senza dimenticare l’importanza della biosicurezza. Soprattutto, si rende indispensabile rendere partecipe tutte le figure professionali coinvolte nell’uso dell’antibiotico, dunque non solo i veterinari ma anche gli allevatori.
Ruolo della farmacodinamica del farmaco per evitare la resistenza batterica
Per decenni, il parametro chiave per suggerire la giusta terapia antibiotica con un farmaco è stata la MIC, ovvero la concentrazione minima di antibiotico capace di inibire o bloccare la crescita di una colonia batterica. Tuttavia, trattandosi della più bassa concentrazione efficace, anche poco al di sotto della sua soglia molti batteri sopravvivono. Più recentemente si prende in considerazione la MPC , ovvero la minima concentrazione di antibiotico capace di bloccare la crescita del batterio meno sensibile in una popolazione ad alta densità. Sopra questa soglia, tutti i batteri vengono inibiti o eliminati. Naturalmente la MPC è generalmente più alta della MIC: tra le due soglie si crea dunque un intervallo (finestra di selezione) all’interno del quale molti batteri vengono bloccati ma non tutti, generando con questa selezione un forte rischio di resistenza. La concentrazione del farmaco somministrato dovrà dunque permanere il meno possibile in questo intervallo, sia durante l’assorbimento della molecola sia durante la sua eliminazione, ed arrivare a superare la soglia della MPC per ottenere una buona terapia con il minore rischio di resistenza batterica. Sembra dunque che la strategia per ridurre drasticamente le resistenze possa essere la somministrazione dell’antibiotico ad alto dosaggio con trattamenti di durata il più breve possibile (Fig.1).
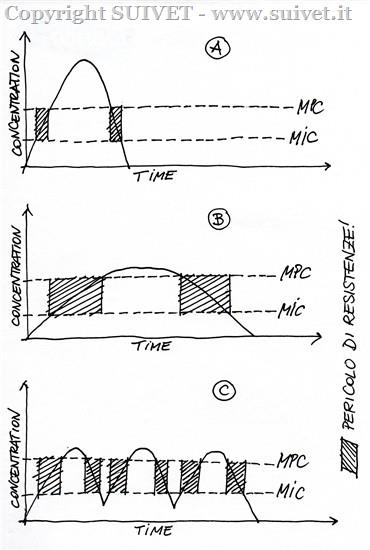
Fig. 1 – L’area tratteggiata rappresenta la permanenza della concentrazione dell’antibiotico all’interno della finestra di selezione. Maggiore è quest’area e maggiore è il pericolo di resistenza batterica. Il farmaco A ha il rischio minore, l’efficacia garantita dal raggiungimento di alte concentrazioni. Il farmaco B garantisce l’efficacia permanendo a lungo in concentrazioni sufficienti, mentre l’efficacia del farmaco C è garantita dalle somministrazioni ripetute. Sia il farmaco B che il C presentano però alto rischio di resistenza batterica.
L’antibiotico come scelta di profilassi: è sempre giustificato?
Il veterinario ricopre un ruolo chiave nella gestione dell’antibiotico e deve avere come fine ultimo la risoluzione di un problema clinico nell’allevamento riducendo però al minimo il rischio di resistenza batterica. Il compito è però delicato e controverso. In tal senso, l’uso profilattico dell’antibiotico va valutato molto attentamente in quanto sospettato di favorire la selezione di resistenza, in particolare nel tratto gastrointestinale. In quali casi il suo uso è giustificato? Nella comunità scientifica (e tra i consumatori!) nascono dibattiti e polemiche.
L’alternativa è la valutazione di una metafilassi, ovvero la somministrazione precoce del farmaco agli animali già esposti al patogeno ma nei quali ancora non si manifesta la patologia se non in alcuni casi sporadici all’interno del gruppo. Sembra ovvio però che non sempre è possibile scegliere la metafilassi al posto della profilassi, come ad esempio in realtà dove l’insorgere di alcune infezioni rappresenta un problema ricorrente e difficilmente controllabile. Diversa la situazione in aziende dove lo stato sanitario è alto, e l’uso profilattico dell’antibiotico può essere discusso a favore della metafilassi. Si conferma ancora una volta l’importanza del veterinario che deve saper scegliere tra metafilassi e profilassi caso per caso a seconda della realtà in cui si trova.
Quando rinunciare all’antibiotico sembra impossibile: i disordini gastrointestinali in svezzamento
Utilizzare gli antibiotici per risolvere i problemi di diarrea, enterite necrotica e E.Coli subito dopo lo svezzamento fa parte delle più comuni scelte di management. D’altra parte questa fase di allevamento è estremamente delicata perché mette a dura prova il tratto gastroenterico dei suinetti, che passano da una dieta lattea digeribile quasi al 100% ad una dieta solida con digeribilità minore. La morfo-fisiologia del digerente, soprattutto negli svezzamenti precoci, non è ancora completamente sviluppata sia in termini di profondità delle cripte e altezza dei villi intestinali che di produzione enzimatica. Il ruolo della flora batterica nella digestione è dunque indispensabile, ma lo stress dello svezzamento mette a rischio il corretto equilibrio tra batteri benefici e batteri patogeni e porta con facilità ai disordini clinici. La somministrazione di antibiotici per via orale rappresenta in molti casi la soluzione a questo squilibrio batterico, ma è opportuno considerare anche eventuali strategie alternative che si fondano sulla manipolazione della dieta.
Probiotici: rappresentano un supplemento alla dieta di microrganismi batterici in grado di alterare la flora intestinale dell’ospite con effetti benefici. Sono rappresentati da bacilli, fermenti e batteri produttori di acido lattico. La loro efficacia è confermata dalla bibliografia scientifica sebbene il loro effetto sia molto variabile a seconda dei dosaggi, del tipo di probiotico, dell’ambiente in cui si trova l’animale che lo assume e della sua dieta.
Prebiotici: sono sostanze che, una volta arrivate alla flora batterica intestinale dell’ospite, ne migliorano l’attività e ne promuovono la crescita. La maggior parte dei prebiotici sono carboidrati non digeribili dall’ospite, rappresentati per lo più da fibre insolubili. La loro efficacia si suppone sia dovuta alla stimolazione del transito intestinale che riduce il tempo per la proliferazone patogena, e al contatto meccanico della fibra sulla mucosa intestinale che provoca un “effetto spazzola” per i batteri adesi sulla superficie. Inoltre la fibra stessa rappresenta un sito di aggancio per i patogeni minimizzando l’infezione dell’ospite.
Livello di proteine nella dieta: è dimostrato che alti livelli di proteina nella dieta in svezzamento predispongano le diarree a causa dell’aumento delle fermentazioni di substrato in digerito nell’intestino. L’uso di bassi livelli di proteina invece migliora la consistenza delle feci, riduce la risposta locale all’infiammazione e diminuisce le diarree. Tuttavia la dieta ipoproteica è discussa perché sembra possa portare a cali di accrescimento, a meno che non sia supportata da una sufficiente aggiunta di amminoacidi essenziali. Recenti ricerche però riportano che la perdita di accrescimento subita in svezzamento dà luogo ad una crescita compensativa successiva, pareggiando le performance e le caratteristiche della carcassa con gli animali alimentati con dieta iperproteica ed antibiotico in svezzamento.